乙烯基芳烃的位置选择性硫羰基化反应
Vera Hirschbeck, Paul H. Gehrtz, and Ivana Fleischer
J. Am.Chem. Soc., DOI: 10.1021/jacs.6b11020
硫酯类化合物在生物医药及有机合成等领域都备受科学家们关注。相对于由醇衍生出的酯而言,硫酯类化合物由于较差的轨道重叠而不太稳定,因而在生物过程及有机合成过程中往往作为中间体存在,例如辅酶A支撑的转移反应过程以及过渡金属催化偶联合成酯、酰胺、醛及酮等过程。
目前,合成硫酯的方法很多,其中最常用放热是通过羧酸、酸酐及酰氯等在活性试剂条件下将硫醇酰基化得到。而另一种方法是过氧化物氧化条件下铜催化醛和硫醇反应得到。此外,还有卤代芳烃的硫羰基化反应等。然而,这些反应或多或少存在反应条件苛刻、低原子经济型、底物不容易制备等缺点。相比之下,烯烃的硫羰基化反应(或称之为氢化硫酯化反应)合成硫酯具有原子经济型和低损耗等优点,而且可以从简单易得的原料开始合成复杂及多反应性分子,如图1所示。而这些反应往往需要高负载的催化剂(3~5mol%)和高温高压(100~100degree,27bar)等缺点,而且也不适用于其他类型的双键类化合物。因而开发普适性的烯烃硫酯化反应迫在眉睫,而迄今为止成功的例子不多。
最近,Ivana Fleischer团队第一次报道了苯乙烯的化学选择性钯催化硫酯化反应,如图1所示。该反应具有反应条件温和(室温、低压)、催化剂低负载(1.0mol%)、高位置选择性及副反应少等优点。
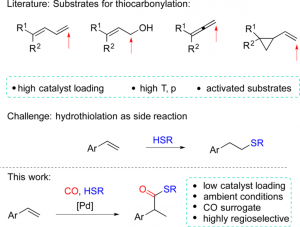

图1,双键的硫羰基化反应







