
椅子构象中的环己烷分子。轴向位置的氢原子以红色显示,而赤道位置的氢原子以蓝色显示。
一环己烷构象是任何数的三维形状,一个的环己烷 分子,同时保持它的完整性可以假定化学键。
的内角的扁平的常规 六边形是120°,而优选的连续键之间的角度在一个碳链为约109.5°时,四面体角。因此,环己烷环倾向于呈现某些非平面(翘曲)构象,其具有接近109.5°的所有角度,因此比扁平六边形形状具有更低的应变能。最重要的形状叫做椅子,半椅子,船和扭船。[1]分子可以很容易地在这些构象之间切换,其中只有两个 – 椅子和扭曲船 – 可以纯净的形式分离。
环己烷构象已经在有机化学中进行了广泛的研究,因为它们是构象异构的典型例子,并且对环己烷的物理和化学性质具有显着影响。
历史背景
1890年,28岁的柏林助手赫尔曼·萨克斯(Hermann Sachse)发表了折叠纸张的说明,表示两种形式的环己烷,他称之为对称和不对称(我们现在称之为椅子和船)。他清楚地知道这些形式有两个氢原子位置(同样,使用现代术语,轴向和赤道),两把椅子可能会互相转换,甚至某些替代品可能会偏向其中一种椅子形式。因为他用数学语言表达了这一切,当时很少有化学家理解他的论点。他曾多次尝试发表这些想法,但都没有成功地捕捉到化学家的想象力。他于1893年去世,享年31岁,这意味着他的想法陷入了默默无闻。仅在1918年,当Ernst Mohr基于最近使用当时非常新的X射线晶体学技术解决的钻石分子结构时[2] [3]能够成功地证明Sachse的椅子是关键的主题。[4] [5] [6] 德里克巴顿和奥德哈塞尔因环己烷和其他各种分子的构象而获得1969年诺贝尔奖。
一般
沿环己烷环的碳 – 碳键是sp 3杂化轨道,其具有四面体对称性。因此,债券之间的角度的四价碳原子具有优选值θ听,说:109.5°。键也具有相当固定的键长 λ。另一方面,相邻的碳原子可以绕键的轴自由旋转。因此,翘曲使得键长和角度接近理想值的环将具有比具有120°角的扁平环更小的应变能。对于碳环的每个特定构造,12碳的方向 – 氢键(因此氢原子的位置)是固定的。
正好有八个扭曲的多边形,其中六个角落的所有内角都等于θ,所有边都等于λ。它们包括两个理想的椅子构造,其中碳交替地位于平均环平面的上方和下方; 和六个理想的船形构造,其中两个相对的碳位于平均平面之上,另外四个位于其下方。理论上,具有任何这些环构象的分子将没有角度应变。然而,由于氢原子之间的相互作用,实际椅子形状的角度和粘合长度与标称值略有不同。出于同样的原因,实际的船形的能量略高于椅子的形状。实际上,船形状是不稳定的,并且自发地变形为扭曲船构造,其是总能量的局部最小值,因此是稳定的。每个稳定的环构象可以在不破坏环的情况下转变成任何其他构象。但是,这种变换必须经过其他具有受压环的状态。特别是,它们必须经历不稳定的状态,其中四个连续的碳原子位于同一平面上。这些形状称为半椅形状。
2011年,Donna Nelson和Christopher Brammer调查了当时使用的综合性本科有机化学教科书,以确定教科书和研究文献之间的一致性; 他们建议修改[ 需要澄清 ]以纠正环己烷构象异构体术语和结构图纸中的不一致性。[1]
椅子构造[ 编辑]
两个椅子构造具有最低的总能量,因此是最稳定的,并且具有D 3d对称性。在基本座椅构造中,碳C1至C6在两个平行平面之间交替,一个具有C1,C3和C5,另一个具有C2,C4和C6。该分子具有垂直于这两个平面的对称轴,并且在绕该轴旋转120°后与其自身一致。两个椅子构造具有相同的形状; 在围绕该轴旋转60°之后,或者在平均平面上镜像之后,一个对另一个是全等的。环在其平均平面上的垂直投影是正六边形。所有CC键相对于平均平面倾斜,但相反的键(例如C1-C2和C4-C5)彼此平行。
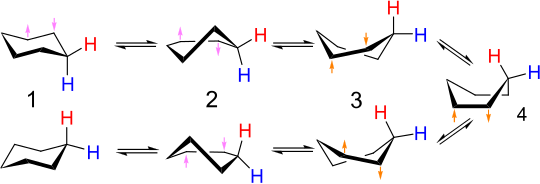
通过船形构造的环己烷椅子翻转(环反转)反应(4)。显示了重要构象的结构:椅子(1),半椅子(2),扭转船(3)和船(4)。当环形翻转完全从椅子到椅子时,先前轴向(蓝色H)转向赤道和轴向(红色H)的氢转向赤道。[7]
由于环翘曲,12个碳 – 氢键中的6个几乎垂直于平均平面并且几乎平行于对称轴,具有交替的方向,并且据说是轴向的。其他六个CH键几乎平行于平均平面,据说是赤道。精确的角度使得每个碳中的两个CH键,一个轴向和一个赤道,相对于对称轴指向相反的方向。因此,在椅子构造中,每种类型有三个CH键 – 轴向“向上”,轴向“向下”,赤道“向上”和赤道“向下”; 每个碳有一个“向上”和一个“向下”,一个轴向和一个赤道。扭转应变。当氢原子被卤素或其他简单基团取代时,通常保留这种几何形状。从一种椅子形状到另一种椅子形状的转换称为环形翻转或椅子翻转。在一种配置中轴向的碳 – 氢键在另一种配置中变为赤道,反之亦然; 但他们的相对位置 – 他们的“向上”或“向下”角色 – 保持不变。在环己烷中,两种椅子构象具有相同的能量,并且在25℃下,环己烷溶液中99.99%的所有分子将处于椅子构象中。
在环己烷衍生物中,取决于取代基的特性和位置,两种椅子构象可具有不同的能量。例如,在甲基环己烷中,最低能量构象是甲基处于赤道位置的椅子。这种配置减少了甲基(碳原子数1)与碳原子3和5的氢原子之间的相互作用; 更重要的是,它避免了两种丁烷相互作用(C1-CH 3键与C2-C3和C5-C6环键)。类似地,顺式 -1,3-二甲基环己烷通常在赤道位置具有甲基,以避免它们之间的相互作用。在六元杂环中例如吡喃,由于异头效应,杂原子旁边的取代基可能更喜欢轴向位置。最后,取代基对赤道构象的偏好是根据其A值来测量的,A值是两个椅子构象之间的吉布斯自由能差,其中取代基位于赤道或轴向位置。正A值表示对赤道位置的偏好。对于非常小的取代基如氘,A值的大小几乎为零,对于非常庞大的取代基如叔丁基,A值的大小为约5kcal / mol 。
其他构造
在基本船形构造(C 2v对称性)中,碳C2,C3,C5和C6是共面的,而C1和C4在相同方向上远离该平面移位。因此,键C2-C3和C5-C6是平行的。在这种形式中,分子具有两个垂直对称平面以及C 2轴。船构造比椅子构造具有更高的能量。特别是两个旗杆氢之间的相互作用产生空间应变。还存在涉及C2-C3和C5-C6键的扭转应变,其被重叠。由于这种应变,船的配置是不稳定的(不是能量函数的局部最小值)。所述扭船式构象,有时也被称为扭[1] (d 2对称性),可以从船式构象通过施加轻微的扭曲至约连接两个独特碳轴进行的分子衍生。结果是具有三个C 2轴且没有对称平面的结构。在室温下扭曲船构象的浓度非常低(小于0.1%),但在1073 开尔文时它可以达到30%。从1073 K到40 K的快速冷却将在大量的扭船构造中冻结,然后在加热时缓慢地转变成椅子构造。[8]半椅构造是一种过渡状态,其 C 2对称性通常被认为是在椅子和扭船之间的路径上。它涉及将一个二面角旋转到零,使得四个相邻的原子是共面的而另外两个原子在平面外
构象之间的相互转换
在室温下,环己烷的两种椅子构象之间存在快速平衡。这两种构象的相互转换一直存在争议,但仍缺乏共识。众所周知,扭船和椅子都是能量极小 – 扭曲船是局部最小值 ; 主席是全球最低限度(基础国家)。[9]
半椅状态(下面的D)是椅子和扭船构造之间的相互转换中的过渡状态。由于扭船的D2对称性,它有两个能量等效路径,它可以采取两种不同的半椅构造,导致环磷烷的两种不同的椅子构造。因此,至少,两个椅子构造之间的相互转换涉及以下顺序:椅子 – 半椅 – 扭曲船 – 半椅’ – 椅子’。
构造涉及以下稳定顺序:椅子>扭船>船>半椅。所有相对构象能量如下所示。[7]
船构造(下面的C)也是过渡状态,允许两种不同的扭船构造之间的相互转换。虽然船形构造对于环己烷的两种椅子构象之间的相互转换不是必需的,但它通常包含在用于描述这种相互转换的反应坐标图中,因为它的能量远低于半椅的能量,因此任何分子都足够从扭船到椅子的能量也有足够的能量从扭船到船。因此,存在多种途径,通过这些途径,扭曲船构象中的环己烷分子可以再次实现椅子构象。
-

构造:椅子(A),扭船(B),船(C)和半椅(D)。能量为43kJ / mol(10.3kcal / mol),25kJ / mol(6kcal / mol)和21kJ / mol(5kcal / mol)。[7]
强迫构象
当取代基或其他结构细节产生构象约束时,例如,当环己烷是桥接化合物的一部分时,环己烷环可被迫采用各种特定的几何形状。一个简单的例子是降冰片烷,其中环己烷部分是船状构象,因为穿过环的碳桥迫使碳1和4比椅子构象允许更接近。Twistane含有四个环己烷环,每个环被迫进入扭曲船构象。
二取代环己烷
|
|
环己烷上的取代发现采用顺式和反式结构,并且不能由简单的单σ键旋转而被容易地切换为具有线性分子。顺式形成意味着两个取代基都存在于碳上2个取代基位置的上侧,而反式意味着它们位于相对侧。尽管环己烷上的碳通过单键连接,但环保持刚性,因为从顺式转换为反式将需要破坏环。cis的命名法被称为(Z),而trans的名称是(E)放在IUPAC名称前面。
对于二取代的环己烷环(即环上的两个基团),两个取代基的相对取向影响可能构象的能量。对于1,2-和1,4-二取代的环己烷,顺式构型导致一个轴向和一个赤道基团。这种配置可以进行椅子翻转。对于1,2-和1,4-二取代的环己烷,反式构型导致轴向两个基团或赤道两个基团。在这种情况下,通过其高空间应变(比平衡器更多的四个相互作用)有效地防止了双轴构象。对于1,3-二取代的环己烷,顺式形式是平衡的,并且翻转的构象在两个轴向基团之间存在额外的空间相互作用。反式 -1,3-二-取代的环己烷像顺式 -1,2-和顺式 -1,4-和能够在两个轴向当量/赤道形式之间翻转。
顺式 -1,4- 二叔丁基环己烷在椅子构象中具有轴向叔丁基,并且转化为扭曲船构象使两组处于更有利的赤道位置。结果,通过NMR光谱测量,在125K下,扭曲舟构象更稳定0.47kcal mol -1(1.96kJ mol -1)。
在去除了空间1,4-氢相互作用的环己烷-1,4-二酮中,实际稳定的构象是扭曲舟。
极性取代基的影响
- 顺式 – 环己烷-1,3-二醇优选双轴构象“氢键内的形成”。
- 2,5- 二叔丁基-1,4-环己二醇存在于船或扭船形式“也是氢键内”
- 2-溴环己酮更喜欢a-Br“min.dipolar repulsion”
- 2-溴-4,4-二甲基环己酮比偶极排斥更喜欢e-Br“1,3双轴相互作用(-ve在e-Br中)[ 需要引证 ]:
- 反式-1,2-二溴环己烷以轴向形式存在于非极性溶剂中“偶极子取消”
在极地溶剂中以赤道形式存在“偶极子增强”。
杂环类似物
存在环己烷的杂环类似物,并且一些具有稳定的扭曲船构象。1,2,4,5-四噻吩是一种有机硫化合物,四个亚甲基桥被硫原子取代,缺乏环己烷不利的1,3-双轴相互作用,其扭曲构象已经存在; 在相应的四甲基结构中,3,3,6,6-四甲基-1,2,4,5-四硫杂环戊烷,扭曲构象实际上占主导地位。







